Микоплазма – возбудитель микоплазмозаПодборка материала и комментарии: ВалераМикоплазмы – это микроорганизмы, занимающие в медицинской классификации промежуточное положение между бактериями, грибами и вирусами.
Микоплазмы имеют маленькие размеры (300 нм), из-за чего они не видны даже в световой микроскоп, у них нет собственной клеточной оболочки, и это сближает их с вирусами.
Точно так же, как вирусы, микоплазмы не могут существовать иначе, чем паразитируя на клетках хозяина, из которых микоплазмы получают основные питательные вещества. Однако, в отличие от вирусов, микоплазмы способны расти в бесклеточной среде.
Микоплазмы – это самые мелкие микроорганизмы, способные жить и размножаться автономно. Размножаются микоплазмы делением и почкованием. Поэтому иногда их рассматривают как переходную ступень от вирусов к одноклеточным микроорганизмам.
В организме человека встречается большое количество видов микоплазм, однако патогенными для человека, то есть при определенных условиях вызывающими болезнь, считаются всего три вида (на самом деле сейчас известно более 5 видов с тенденцией к росту числа новых претендентов на роль патогенов) этих микроорганизмов:
• Mycoplasma hominis
• Mycoplasma genitalium
• Mycoplasma pneumoniae
Все эти виды микоплазм паразитируют, как правило, на клетках эпителия – слизистой оболочки, выстилающей стенки кишечного, дыхательного и мочеполового трактов.
Болезнь может возникнуть либо при ослаблении иммунной системы хозяина, либо при сочетании патогенных типов микоплазмы с другими патогенными микроорганизмами.
Болезнь, вызываемая микоплазмами – микоплазмоз – поражает либо дыхательную систему, вызывая воспалительные заболевания горла, бронхов легких, либо мочеполовой тракт. В последнем случае мы имеем дело с урогенитальным (или мочеполовым) микоплазмозом, который в настоящее время является достаточно распространенным заболеванием среди инфекций, передающихся половым путем (ИППП)
Как правило, у женщин микоплазмы колонизируют влагалище, уретру и шейку матки, а у мужчин – уретру и крайнюю плоть, вызывая инфекционно-воспалительный процесс.
Кроме того, известно, что у мужчин микоплазмы способны подавлять активность сперматозоидов, а в некоторых случаях даже вызывать их гибель. Кроме своего «основного действия», микоплазмы способны оседать в суставной жидкости и вызывать воспаление суставов.
Собственно говоря, токсичными для человека являются не сами микоплазмы, а продукты их жизнедеятельности, которые повреждают стенки клеток эпителия, а, кроме того, утилизируют холестерин и жирные кислоты клетки хозяина.
Впервые микоплазмы были выделены среди других микробов при микроскопических исследованиях у женщин еще в 1937 году, а у мужчин позже – в 1958 году, но то, что именно они вызывают определенное воспаление, было подтверждено лишь в 1979 году.
До сих пор до конца не выяснено, каким способом Mycoplasma hominis прикрепляется к клеткам эпителия. Известно, что эта связь достаточно прочная, но полного прикрепления к клетке, как это бывает у многих вирусов, не происходит. Прочную связь с хозяином обеспечивают несколько факторов: сходство строения клеточной мембраны микоплазмы с мембранами организма-хозяина, отсутствие клеточной стенки и малые размеры микоплазм. Кроме того, внедрение микоплазм в мембрану клеток организма-хозяина делает их более защищенными от воздействия иммунной системы хозяина.
К внешней среде микоплазмы неустойчивы – вне организма хозяина они быстро гибнут, поэтому заражение микоплазмами происходит, как правило, либо половым путем, либо при тесных бытовых контактах.
Бытовым путем заражение происходит через предметы личной гигиены (белье, купальники, полотенца, постель). Возможна вертикальная передача микоплазмоза – передача микоплазмоза во время родов.
Ранее академические круги решили, что если микоплазмы широко распространены в природе (встречаются у растений, животных и человека - всего по разным оценкам от 40 до 100 разновидносткей) и в латентной форме обнаруживаются у 20-50% людей, то они не представляют опасности для здоровья. Не было вначале понимания природы микоплазм. И за период открытия немногим более полувека считается что микоплазмы до сих пор плохо изучены. Несмотря даже на то, что к настоящему времени расшифрован геном некоторых микоплазм:
В Лаборатории молекулярной биологии (Гейдельбергский университет) под руководством профессора Р. Геррманна (R. Herrmann) для секвенирования был выбран геном M. pneumoniae размером около 800 т. п. о. За три года напряженной работы лаборатории поставленная задача была решена ( Himmelreich et al., 1996 ). Авторы впервые сконструировали космидную библиотеку, а затем секвенировали космиды и расположили их в исходном порядке, так что геном M. pneumoniae был неоднократно прочтен в обоих направлениях ( Himmelreich et al., 1996 ). Однако группа Р. Геррманна оказалась не первой, представившей полную нуклеотидную последовательность генома микоплазмы.
До конца 1994 г. многие молекулярные биологи полагали, что первым полностью прочитанным геномом будет геном бактерии Escherichia coli размером 4720 т. н. п., но первым был прочтен геном бактерии Haemophilus influenzas длиной 1830 т. н. п. ( Fleischmann et al., 1996 ) в Институте геномных исследований (TIGR), который являлся одним из главных исполнителей международной программы "Геном человека" . Почти одновременно сотрудники этого института приступили к расшифровке генома микоплазмы - M. genitalium .
Что такое микоплазмозМикоплазмоз – это острое или хроническое инфекционное заболевание. Микоплазмоз вызывают микоплазмы.
В организме человека могут существовать свыше 17 видов микоплазм.
Сейчас уже доказано, что не менее четырёх из них является патогенами
(ранее в целом микоплазмы не рассматривались как патогены).
В зависимости от возбудителя, микоплазмоз может быть мочеполовым или респираторным.
Респираторный микоплазмоз протекает, как правило, в форме ОРЗ или, в тяжелых случаях, пневмонии. Передается респираторный микоплазмоз воздушно-капельным путем. К симптомам можно отнести повышение температуры, воспаление миндалин, насморк, в случае перехода микоплазменной инфекции в пневмонию налицо бывают все признаки воспаления легких: озноб, повышение температуры, симптомы общей интоксикации организма.
Мочеполовой микоплазмоз – это инфекция мочеполового тракта, передающаяся половым или, реже, бытовым путем.
Микоплазмы выявляются в 60-90% случаев появления воспалительной патологии мочеполовой системы. Кроме того, при анализе на микоплазмоз здоровых людей, микоплазмы обнаруживаются в 5-15% случаев. Это говорит о том, что довольно часто микоплазмоз протекает бессимптомно, и ничем не проявляет себя до тех пор, пока иммунная система человека обладает достаточной устойчивостью.
Однако при таких обстоятельствах, как беременность, роды, аборт, переохлаждение, стрессы, микоплазмы активизируются, и болезнь переходит в острую форму.
Преобладающая форма мочеполового микоплазмоза считается – это хроническая инфекция с малосимптомным и замедленным течением.
Микоплазмоз может спровоцировать такие заболевания как пиелонефрит, простатит, уретрит, артрит, сепсис, различные патологии беременности и плода, послеродовой эндометрит.
Микоплазмоз распространен во всем мире.
Наиболее часто микоплазмозом страдают женщины, которые перенесли гинекологические заболевания, инфекции, передающиеся половым путем, или ведущие беспорядочный образ жизни.
В последнее годы участились случаи микоплазмоза у беременных, что отчасти связано с тем, что во время беременности иммунитет женщины бывает несколько ослаблен и через эту «брешь» в организм проникает инфекция. Вторая причина «увеличения» доли микоплазмозов – современные методы диагностики, которые позволяют выявить «скрытые» инфекции, которые неподвластны простым методам диагностики таким как мазок.
Микоплазмоз для беременных – очень нежелательное заболевание, которое может привести к выкидышу или замершей беременности, а также к развитию эндометрита – одного из наиболее серьезных послеродовых осложнений.
Диагностика микоплазмозаТак как признаков, характерных именно для микоплазмоза, нет, а размеры микроорганизмов не позволяют увидеть их при микроскопии (обычный мазок), диагностика микоплазмоза проводится только с помощью лабораторных методов и является достаточно сложной.
Сложившееся исторически неверное отношение к микоплазмам как не опасным микроорганизмам трудно преодолеть в психологии и сознании людей.
В последние годы появилось много научных статей показывающих, что микоплазмы - это страшный паразит от которого достаточно тяжело вылечиться полностью. (Как например в случае микобактерий Коха -туберкулёз. В последнее время наблюдается рост заболеваемости в том числе в России туберкулёзом. Часты стали случаи лекарственно устойчивых форм туберкулёза). Как и микоплазмы микобактерии туберкулеза относят к внутриклеточной инфекции, с чем связывают их высокую способность к персистенции. Первично инфицируют макрофаги хозяина, развивая особые стратегии выживания и размножения в этих высокоспециализированных клетках. Используя способность макрофагов образовывать специализированные органеллы — фагосомы, микобактерии приспособили эти органеллы для своей жизнедеятельности, при этом получая несомненные преимущества, необходимые для избегания действия защитных «хозяйских» механизмов, таких как антитела и др.
Есть сведения о том что микоплазмы способствуют развитию рака, путём ослабления иммунитета. Микоплазмы, токсоплазмы, микоз грибковый и др. разновидности обнаруживаются почти в 95% случаев у больных раком. Известны случаи (медицинский центр Елисеевой) когда лечение направленное против паразитов приводило к прекращению развития раковой опухоли на ранних стадиях.
Например, микоплазмы в хронически инфицированных клетках подавляют стауроспорин - индуцированный апоптоз, что является онкогенным признаком. То есть паразитируя (чаще всего в цитоплазме) внутри клетки микоплазмы не дают ей уйти в апоптоз (программируемая гибель) что ведёт к росту опухоли.
Так же серьёзной проблемой является наличие у микоплазм (токсоплазм) способности образования цист устойчивых к внешним факторам и антибиотикам, микоплазмы в состоянии цист способны длительное время "пережидать" возникшие неблагоприятные для них условия.
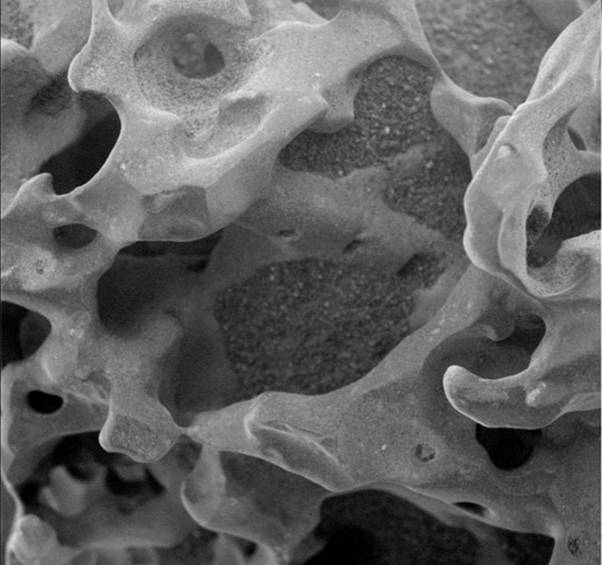
Фотографии микоплазм

- Микоплазма_1.jpg (23.34 КБ) Просмотров: 48321
Ureaplasma urealyticum (розовоокрашенные везикулы): инфицированный (снизу) и слабоинфицированный (сверху) эпителиоциты. Объектив 90х.

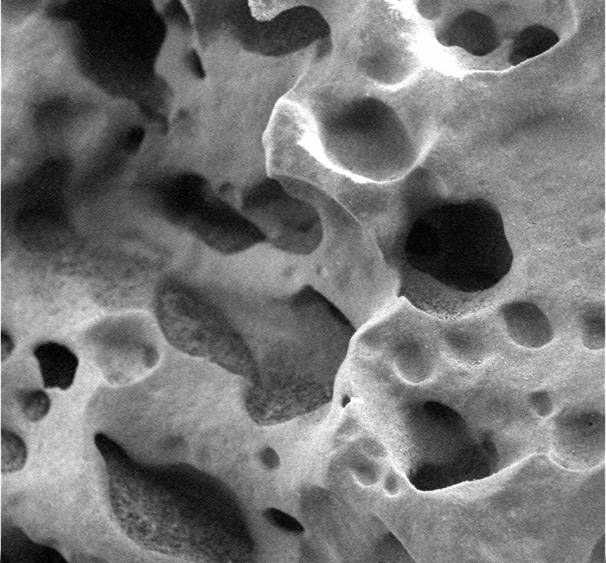
- Микоплазма_2.jpg (14.18 КБ) Просмотров: 48321
Лейкоциты с микоплазменными включениями (слабоокрашенные везикулы) и структурными дефектами, морфологически сходными с таковыми при некоторых лейкозах (возможно, вызваны ретровирусами). Объектив 90х.В целом патогены класса микоплазм можно рассматривать как угрозу здоровья нации.
И в ряде случаев можно рассматривать как фактически биологическое оружие.
Особенно на фоне происходящих в мире событий.
12-ая Международная Конференция.(2004г.)
Влияние некоторых видов микоплазм на развитие ВИЧ - инфекции in vitro Ставцев М. Г. ГУ НИИЭМ им. Н. Ф. Гамалеи, РАМН, Москва, Россия. Общим для ВИЧ-инфекции и микоплазменной инфекции in vivo и in vitro в равной мере является развитие разнообразных и тяжелых дефектов иммунной системы, признанных ведущим фактором патогенеза заболеваний, вызываемых этими патогенами. Было также показано, что
микоплазма M.incognitus может быть ко-фактором в прогрессии СПИД'a (C.- H. Lo, et al., 1991-1993).
Целью работы явилось исследование влияния
4 видов микоплазм, обладающих разным уровнем патогенности и являющихся наиболее распространенными причинными агентами разнообразных патологий у людей, на развитие и течение ВИЧ-инфекции в Т-лимфоцитах периферической крови людей in vitro.
Влияние микоплазм на пролиферативные функции Т-клеток в условиях моно- и ко-инфекции с ВИЧ-1 измеряли по включению радиоактивной метки 3Н-ТТР. Экспрессию a-INF определяли в ИФА с помощью тест-системы "Prokon". Продукцию р24-антигена ВИЧ в культуральной жидкости измеряли в ИФА с помощью тест-системы Vironostika. Определение экспрессии гена MPNI42, кодирующего продукцию трансмембранного белка адгезина Р1 у M. pneumoniae осуществляли методом RT PCR.
Полученные результаты свидетельствуют о способности, как минимум, двух видов микоплазм стимулировать пролиферацию первичных Т-лимфоцитов и их выживаемость. При этом стимулирующий эффект связан преимущественно с живыми клетками микоплазм, а не с фильтратами их среды культивирования. Установлено двукратное увеличение продукции р24-антигена ВИЧ в клетках при ко-инфекции с M.pneumoniae и M.arthritidis. Обнаружена индукция синтеза a-INF в Т-клетках, смешанно инфицированных ВИЧ и микоплазмой, на ранних стадиях инфекции M.pneumoniae. Не выявлено количественных различий в проявлении перечисленных эффектов между патогенными и непатогенными видами микоплазм. В частности, не выявлено зависимости в характере влияния на течение ВИЧ-инфекции от наличия или отсутствия главного фактора патогенности у М.pneumoniae белка адгезина Р1.
Полученные данные позволяют говорить о наличии стимулирующего влияния некоторых микоплазм на течение ВИЧ-инфекции в Т-лимфоцитах, по крайней мере, в границах исследованных параметров.
________________________________________
Можно отметить непропорциональное (неадекватное) внимание в обществе уровню существующей угрозы (проблемы).
Например ниже привожу официальную карту по распространению туберкулёза в мире.
Ежегодно в мире заболевают туберкулезом более 8 миллионов человек и умирают – около 2 миллионов человек . Эпидемия ширится и становится все более опасной. Недостатки в работе системы здравоохранения, распространение ВИЧ-инфекции/СПИДа и развитие лекарственно – устойчивых форм туберкулеза – все это способствует развитию эпидемии.
 Ниже привожу выдержки из научной публикации в журнале "Клиническая Микробиология и Антимикробная Химиотерапия". №2 2000 г по возбудителям атипичной пневмонии:Современные подходы к диагностике атипичных пневмоний
Ниже привожу выдержки из научной публикации в журнале "Клиническая Микробиология и Антимикробная Химиотерапия". №2 2000 г по возбудителям атипичной пневмонии:Современные подходы к диагностике атипичных пневмонийИ.С. Тартаковский
Институт эпидемиологии и микробиологии им. Н.Ф.Гамалеи РАМН, МоскваВозбудители атипичных пневмоний - микоплазмы, легионеллы, хламидии, Coxiella burnetii (возбудитель лихорадки Ку) - играют заметную роль в инфекционной патологии человека. Несмотря на существенные различия в биологии возбудителей, эпидемиологии и клинике инфекционного процесса, данную группу микроорганизмов объединяют устойчивость к пенициллинам и другим бета-лактамам, а также общие подходы к лабораторной диагностике. Наибольшее значение для лабораторной диагностики атипичных пневмоний в настоящее время приобретают иммунологические и молекулярно-биологические методы (иммуноферментный анализ, иммунофлюоресценция, полимеразная цепная реакция). Носительство и персистенция, характерные для инфекций вызываемых данной группой возбудителей, обусловливают необходимость особенно тщательной интерпретации серологических реакций и результатов молекулярно-биологических методов исследования. Дальнейшее совершенствование лабораторной диагностики атипичных пневмоний связано с поиском новых специфичных антигенных и нуклеотидных маркеров возбудителей, постановкой этиологического диагноза в начальной фазе заболевания, снижением стоимости наиболее чувствительных диагностических тест-систем.
Ключевые слова: атипичные пневмонии, микоплазмы, легионеллы, хламидии, коксиелла, диагностика.
Введение
Термин "первичные атипичные пневмонии" вошел в практику в 40-е годы XХ века и использовался для характеристики пневмоний, плохо поддающихся лечению сульфаниламидными препаратами и пенициллином. Первым этиологическим агентом данной группы был выделен из мокроты больного пневмонией фильтрующийся возбудитель, названный агентом Итона. Предположение о вирусной природе данной группы пневмоний плохо согласовывалось с чувствительностью к тетрациклину, а выделение агента Итона на искусственной питательной среде доказало, что возбудитель не является вирусом. Агент Итона был отнесен к группе плевропневмониеподобных микроорганизмов, известных еще с 1898 г., после выделения их от крупного рогатого скота. В 1963 г. название агент Итона было заменено на современное видовое - Mycoplasma pneumoniae [4,6].
В последние годы группа "атипичных пневмоний" пополнилась очень разными по своей биологии возбудителями, не имеющими ничего общего с позиций таксономии прокариотов. Вызываемые ими инфекции существенно отличаются по клинике, эпидемиологии, условиям циркуляции возбудителя и путям их передачи. Несмотря на эти обстоятельства, термин "атипичные пневмонии", не являясь строго научным определением, входящим в Международную классификацию болезней, достаточно прочно вошел в клиническую и микробиологическую практику [8].
Основные возбудители атипичных пневмоний
Микоплазмы - M.pneumoniae
Хламидии - C.pneumoniae, C.trachomatis, C.psittaci
Легионеллы - L.pneumophila
Возбудитель лихорадки Ку - C.burnetii
Группу возбудителей атипичных пневмоний объединяет устойчивость к пенициллину и другим бета-лактамам, а жизнеспособность самого термина связана с широким распространением данных инфекций.
Оценка эффективности любого нового препарата для антимикробной терапии пневмоний практически невозможна без анализа его действия против возбудителей атипичных пневмоний.
Наконец, общими для атипичных пневмоний являются методические подходы к лабораторной диагностике, связанные с длительным и требующим специальной подготовки выделением культуры возбудителя и ведущей в настоящее время ролью иммунологических методов диагностики [3].
Возбудители атипичных пневмоний и их этиологическое значение
Хотя возбудитель респираторного микоплазмоза был выделен в 40-е годы, активное изучение биологии возбудителя и эпидемиологии инфекции были начаты только в 60-е годы. Микоплазменные пневмонии, по данным ВОЗ и ряда отечественных исследователей, составляют 10-20% от общего числа пневмоний, а в изолированных и полуизолированных коллективах (военнослужащие, школьники, воспитанники детских учреждений) - до 50% [4,6,21]. Скопление людей, наличие тесных и долговременных контактов создают благоприятные условия для циркуляции возбудителя, распространяющегося воздушно-капельным путем, что приводит к высокому уровню инфицирования членов коллектива. Наиболее часто клинически выявляется микоплазменная пневмония средней тяжести.
Данные серологических исследований свидетельствуют о значительном числе бессимптомных форм или носительстве. Источником инфекции могут быть как больные, так и люди с бессимптомными формами микоплазмоза. Эпидемии респираторного микоплазмоза могут развиваться медленно с постепенным вовлечением в эпидемический процесс отдельных членов коллектива в течение 9, 18 и более месяцев.
Микоплазмы являются самыми мелкими по размерам среди внеклеточно культивируемых патогенных микроорганизмов. К основным биологическим особенностям микоплазм, определяющим их место среди других прокариотов, а также во многом определяющим их эпидемиологическое значение и подходы к диагностике и лечению, относятся:
1. отсутствие ригидной клеточной стенки, что обусловливает полиморфизм клеток; резистентность к различным агентам, подавляющим синтез клеточной стенки, прежде всего к пенициллину и другим бэта-лактамам;
2. малый размер генома - около 500 мДа (наименьший для прокариот), что обусловливает ограниченность биосинтетических возможностей и высокие требования к условиям культивирования;
3. микоплазмы - уникальные мембранные паразиты, способные к длительной персистенции; прочно связываясь с мембраной инфицированной эукариотической клетки, микоплазмы "ускользают" от фагоцитоза. Способность паразитировать на мембране эукариотической клетки исключительно важна для понимания патогенеза инфекции, вызванной M.pneumoniae
Возбудитель легионеллеза, Legionella pneumophila, впервые выделенный и идентифицированный в 1977 г. после крупной эпидемической вспышки пневмоний в Филадельфии (США) с 15% летальным исходом, активно изучается в последние годы. Частота легионеллезной инфекции среди внебольничных пневмоний варьирует от 1 до 15% [3,5,15]. Более низкий процент свидетельствует об отсутствии эффективной диагностики, более высокий - о наличии эндемичных очагов и благоприятных условий для аэрогенного заражения легионеллами.
L.pneumophila - распространенный в природе гидрофильный микроорганизм, в природных водоемах паразитирующий в амебах и инфузориях. В системах водоснабжения, кондиционирования воздуха, иных инженерно-технических системах, связанных с циркуляцией воды, происходит колонизация легионеллами различных металлических, резиновых и синтетических поверхностей. При высокой концентрации возбудителя в таких системах в сочетании с возможностью аэрозольного распространения весьма вероятно возникновение легионеллезной инфекции.
Легионеллез не контагиозен, то есть заражение от человека практически невозможно. Помимо основного аэрозольного пути заражения возможна и аспирация как путь передачи при внутрибольничных легионеллезных пневмониях у больных на фоне иммуносупрессии. Подозрение на легионеллезную инфекцию возникает в случае острой, тяжелой, как правило, лoбарной пневмонии, плохо поддающейся лечению пенициллинами и другими бета-лактамами.
L.pneumophila - единственный возбудитель атипичных пневмоний, для которого отсутствуют данные о носительстве и персистенции.
L.pneumophila - грамотрицательная палочка размером 0,5-0,7 Х 2,5 мкм, не образующая спор и капсул. Легионеллы не ферментируют углеводы, будучи хемоавтотрофами, в качестве источника углерода и энергии используют аминокислоты. В организме человека легионеллы размножаются преимущественно в альвеолярных макрофагах, полиморфно-ядерных нейтрофилах и моноцитах крови.
Биология легионелл не столь своеобразна, как у хламидий и микоплазм. Будучи факультативными внутриклеточными паразитами, легионеллы не растут на обычных питательных средах, используемых в клинической микробиологии, таких, как кровяной агар и агар МакКонки, что связано с потребностью возбудителя в L-цистеине и растворимом пирофосфате железа (Fe +++) и высокими требованиями к рН среды - 6,95.
Стандартная среда для выделения легионелл - агар BCYEальфа, который содержит дрожжевой экстракт, L-цистеин, соединения железа, альфа-кетоглутарат и АСES [N-(2-ацетамидо)-2-аминоэтансульфоновая кислота]-буфер.
Хламидии - облигатные внутриклеточные паразиты. В инфекционной патологии человека играют заметную роль в качестве возбудителя трахомы и паратрахомы, урогенитальных инфекций, респираторных заболеваний и пневмоний, а также ряда других заболеваний. В 90-е годы наибольший научный интерес проявился в выяснении значимости хламидий в этиологии пневмоний. Это обусловлено открытием вида Chlamydia pneumoniae (или по измененной недавно классификации - Chlamydophila pneumoniae), который до 1989 г. описывали как TWAR [2,10].
Эпидемиологические исследования в США, Финляндии и других странах свидетельствуют, что C.pneumoniae вызывает около 10-12% пневмоний [21]. Для инфекции характерно клиническое течение средней тяжести, но возможно и тяжелое с летальным исходом. Тяжелое течение чаще наблюдается у пожилых и лиц с хроническими заболеваниями. Как и Mycoplasma pneumoniae, C.pneumoniae нередко вызывает эпидемические вспышки в закрытых коллективах. Помимо пневмоний возбудитель вызывает фарингиты, бронхиты, синуситы и гриппоподобные заболевания. Другим видам хламидий также принадлежит заметная роль в этиологии пневмоний (C.trachomatis, возбудитель урогенитального хламидиоза вызывает до 20% пневмоний у новорожденных).
Если C.trachomatis и C.pneumoniae вызывают антропонозный хламидиоз, то вид C.psittaci является возбудителем зоонозных хламидиозов, пeредающихся человеку при контакте с птицами. В клинической картине орнитоза ведущее место также принадлежит пневмонии. Количество орнитозных пневмоний в последние годы невелико - 1-3%, но достаточно стабильно.
Являясь облигатными внутриклеточными паразитами, хламидии не могут размножаться вне клеток макроорганизма. Поэтому они не могут быть выделены на искусственной питательной среде.
Для диагностики и лечения хламидиозов имеют значение следующие особенности их биологии.
1. Хламидии по строению сходны с грамотрицательными бактериями, имеют цитоплазматическую мембрану и клеточную стенку.
2. В клетках макроорганизма хламидии образуют цитоплазматические включения, состоящие в основном из 2 форм микробных клеток: элементарных телец диаметром 0,25-0,35 мКм (инфекционные формы) и ретикулярных телец (вегетативные формы) диаметром 0,5-1 мКм. Элементарные тельца адаптированы к внеклеточному выживанию, метаболически малоактивны. Ретикулярные тельца быстро разрушаются во внешней среде, чувствительны к антибиотикам, в клетках хозяина проявляют высокую метаболическую активность.
3. Уникальный цикл развития хламидий связан с проникновением в клетку путем фагоцитоза элементарных телец, которые через переходные формы преобразуются в ретикулярные тельца. Размножившиеся путем бинарного деления ретикулярные тельца преобразуются в элементарные тельца нового поколения. Цикл, продолжающийся 40-72 ч, завершается разрывом мембраны включений и клетки хозяина. Содержимое включений поступает во внеклеточную среду, и элементарные тельца заражают новые клетки. При диагностических исследованиях хламидии выявляют внутри пораженных клеток в виде включений либо вне клеток в виде элементарных и ретикулярных телец.
4. Помимо продуктивного цикла для хламидий возможна и длительная их персистенция без выраженной симптоматики.
Лихорадка Ку, известная с конца 30-х годов, также может быть отнесена к группе атипичных пневмоний [1,16]. Хотя возбудитель Coxiella burnetii вызывает не более 1-3% от числа пневмоний, в эндемичных районах дифференциальная диагностика Ку лихорадки необходима для представления о реальной этиологической структуре и эффективной терапии пневмоний.
В эндемичных для лихорадки Ку регионах частота вызываемых ею пневмоний значительно выше и может достигать 7-10% (провинция Баскония в Испании, Новая Шотландия в Канаде, Южная Франция) [16,23].
Основным источником C.burnetii для человека является домашний крупный и мелкий рогатый скот. Для лихорадки Ку характерны множественные пути передачи: аспирационный, контактный, алиментарный, трансмиссивный, но в основном заражение происходит при вдыхании инфицированных аэрозолей.
Главные факторы риска связаны с уходом за животными и обработкой продуктов животноводства. C.burnetii - облигатный внутриклеточный паразит со строением клеточной стенки, типичной для грамотрицательных бактерий. Для морфологии коксиелл характерен выраженный плеоморфизм с преобладанием бациллярных форм размером 0,25 х 1,5 нм. У С.burnetii описаны две антигенные фазы, различающиеся антигенными свойствами. C.burnetii в естественных условиях циркуляции принадлежит к фазе I, в начальный период инфекции переходит в антигенную фазу II.
Методы диагностики атипичных пневмоний
Для лабораторной диагностики атипичных пневмоний можно использовать 4 группы методов:
1. морфологические, основанные на выявлении характерных морфологических структур возбудителя непосредственно в клиническом материале;
2. культуральные, основанные на выделении возбудителя на питательной среде, культуре клеток или куриных эмбрионах;
3. иммунологические, основанные на выявлении антигенов возбудителя и антител к ним;
4. молекулярно-биологические, основанные на определении специфичных нуклеотидных последовательностей.
Для выделения M.pneumoniae из клинического материала (мокрота, плевральная жидкость, легочная ткань, смывы с задней стенки глотки) требуются исключительно богатые среды, содержащие все предшественники, необходимые для синтеза макромолекул, способные обеспечить микоплазмы источниками энергии, удовлетворяющие их потребность в стеролах и фосфолипидах.
Осмотическое давление среды для лишенных ригидной клеточной стенки микоплазм, достигаемое за счет ионов калия и натрия, также является необходимым условием их роста. Несмотря на столь богатый состав среды, M.pneumoniae растет крайне медленно, требует 7-14 сут, а часто и гораздо более длительных сроков инкубации. Богатый состав среды и длительные сроки инкубации могут привести к контаминации посева другими, менее требовательными к условиям культивирования, ахолеплазмами и микоплазмами. Наконец, с учетом способности M.pneumoniae к персистенции ее выделение не является 100% подтверждением острой микоплазменной инфекции [21,29].
Поэтому в практических лабораториях для диагностики M.pneumoniae-инфекции наибольшее распространение получили иммунологические методы, основанные на выявлении в клиническом материале микоплазменных антигенов или определения специфических антител к ним.
Наиболее распространенной и апробированной является реакция иммунофлюоресценции, позволяющая выявлять микоплазменные антигены в мазках из носоглотки, мокроты и другом клиническом материале. Данный метод обладает высокой специфичностью и значительно более высокой чувствительностью, чем культуральные методы. Антиген M.pneumoniae может быть обнаружен также в сыворотке крови больных. Для этого используют реакцию агрегат-гемагглютинации и иммуноферментный анализ [6,7].
Реакция агрегат-гемагглютинации позволяет выявить наличие антигена микоплазм в сыворотке крови больного в концентрации 0,001-0,0001 мг/л. Особенность реакции заключается в том, что для сенсибилизации эритроцитов используют агрегированные глутаратальдегидом белки иммунной сыворотки. При этом антитела вводятся в состав трехмерных белковых комплексов, вследствие чего часть активных центров антител отделяется от поверхности эритроцита и становится более доступной для детерминант антигена. Минимальный диагностический титр составляет 1:8. Иммуноферментный метод позволяет выявлять антиген в сыворотке крови в минимальном диагностическом титре 1:200.
Исключительно важным для диагностики M.pneumoniae-инфекции является исследование на наличие специфических антител к гликолипидному или поверхностному белковому антигену микоплазм [21]. Диагностическое значение имеет нарастание титров антител в динамике болезни в 4 и более раз в парных сыворотках крови. Для выявления антител используют реакцию связывания комплемента (РСК), реакцию непрямой гемаглютинации (РНГА) и иммуноферментный анализ (ИФА). Диагностическое нарастание титров антител обычно удается выявить не ранее чем через 2-3 нед болезни. Ряд современных тест-систем позволяет выявлять специфические IgM антитела в ранние сроки болезни [13,14].
Для иммунологической диагностики M.pneumoniae-инфекции существенно и то обстоятельство, что при затяжной вялотекущей микоплазменной пневмонии значительное количество антигенов микоплазм может находиться в составе циркулирующих иммунных комплексов. Диссоциация таких комплексов в сыворотке крови с помощью буфера (рН 2,4) позволяет выявлять антигены микоплазм в высоких титрах.
Следует учитывать, что антигенное родство M.pneumoniae с тканями человека и животных, оказывая прямое воздействие на иммунный ответ хозяина, может не только вызывать аутоиммунную реакцию, но и приводить к ложноположительным результатам при серологических исследованиях.
В последние годы активно разрабатываются молекулярно-биологические методы, основанные на выявлении специфичных нуклеотидных последовательностей ДНК микоплазм. РНК-зонды или ПЦР-диагностические тест-системы выявляют обычно нуклеотидные последовательности 16S рРНК или гена, кодирующего синтез белка адгезии р1 [26,11]. Методы отличаются высокой чувствительностью и теоретически позволяют выявлять единичные клетки микоплазм. Практическое применение этих методов требует особо тщательной постановки реакции с учетом возможной контаминации клинического материала, носительства или персистенции возбудителя. Вследствие этого методы не всегда отличаются высокой специфичностью.
Проблемы и перспективы диагностики атипичных пневмоний
Приведенные данные подтверждают заметное место возбудителей атипичных пневмоний в инфекционной патологии человека и свидетельствуют об общности методических подходов к диагностике столь гетерогенной группы инфекций. Значительный прогресс в разработке иммунологических и молекулярно-биологических методов позволяет эффективно осуществлять комплексную дифференциальную диагностику атипичных пневмоний не только в специализированных научных центрах, но и в практических бактериологических или иммунологических лабораториях здравоохранения. При этом необходимо учитывать следующие общие проблемы, возникающие при диагностике данной группы инфекций [3,9].
1. Носительство и персистенция, характерные для микоплазм, хламидий и коксиелл, не всегда позволяют считать окончательным подтверждением диагноза даже выделение культуры возбудителя, не говоря уже о выявлении суммарных антител или нуклеотидных последовательностей.
2. При пневмониях может иметь место смешанная инфекция. По нашим данным, до 20% выявленных пневмоний имеют смешанную этиологию с участием возбудителей атипичных пневмоний [27]. Описаны ассоциированные инфекции M.pneumoniae и C.pneumoniae или L.pneumophila и M.pneumoniae. В данном случае общность методических подходов облегчает правильный диагноз и выбор полиэтиотропного лечения.
3. Перекрестно реагирующие антитела и последовательности нуклеотидов часто ограничивают возможности высокочувствительных и специфичных методов диагностики. В качестве примера можно привести метод ИФА для выявления растворимого антигена L.pneumophila в моче. Дорогостоящие тест-системы фирм "Binax" или "Biotest" позволяют эффективно выявлять антиген только 1-й серогруппы L.pneumophila. Хотя более 70% случаев легионеллезных пневмоний связаны именно с этой серогруппой, попытки создать аналогичную тест-систему для остальных 14 серогрупп L.pneumophila пока безуспешны из-за перекрестных серологических реакций.
4. Высокие требования к условиям постановки реакций, оборудованию, стерильности, подготовке персонала и т.д. необходимо соблюдать при применении иммунологических и молекулярно-биологических методов диагностики. В противном случае достоинства данной группы могут дать обратный результат - высокий процент ложноположительных реакций. Контаминация исследуемого материала одной клеткой постороннего возбудителя при постановке ПЦР может привести к неправильному диагнозу.
На наш взгляд, применение двух взаимодополняющих методов является оптимальным подходом для подтверждения диагноза инфекции, вызванной любым возбудителем атипичных пневмоний. Так, выявление высокого уровня антител к M.pneumoniae в сыворотке крови в сочетании с выявлением антигена в крови в реакции агрегат-гемагглютинации или его обнаружением в отделяемом респираторного тракта методом иммунофлюоресценции или ПЦР позволяет достоверно подтвердить диагноз M.pneumoniae-инфекции. Сравнительные исследования показывают эффективность такого подхода и для диагностики хламидийных пневмоний [12,13,20,28,29].
При выборе диагностических препаратов существенное значение имеет и экономический фактор. В ряде случаев применение двух простых и недорогих взаимодополняющих методов может быть более эффективным, чем использование дорогостоящей тест-системы с высоким уровнем чувствительности и специфичности. Так, выявление антител в высоких титрах к L.pneumophila в непрямой иммунофлюоресценции в сочетании с выявлением возбудителя в отделяемом респираторного тракта в прямой иммунофлюоресценции более надежно для подтверждения легионеллеза, чем применение более дорогостоящих методов ПЦР или иммуноферментного анализа.
Для дальнейшего совершенствования методической базы диагностики атипичных пневмоний наибольшее значение имеют:
1. поиск новых высокоспецифичных антигенных и нуклеотидных маркеров, позволяющих избежать перекрестных реакций на уровне вида или серовара возбудителя;
2. совершенствование методов, выявляющих острую фазу заболевания (определение IgM антител при хламидийной и микоплазменной инфекциях, определение растворимого антигена в моче при легионеллезе и т.д.);
3. снижение стоимости наиболее чувствительных и специфичных тест-систем, лимитирующей их широкое использование в практических лабораториях.
Литература
1. Дайтер А.Б., Тарасевич И.В. Лихорадка Ку. Руководство по эпидемиологии инфекционных болезней. 1993. с.333-42.
2. Мартынова В.Р., Колкова Н.И., Шаткин А.А. Хламидии и хламидиозы: клиника, биология и диагностика. Рос мед вести 1997;3:49-55.
3. Покровский В.И., Прозоровский С.В., Малеев В.В., Тартаковский И.С. Этиологическая диагностика и этиотропная терапия острых пневмоний. М:Медицина;1995.
4. Прозоровский С.В., Васильева В.И., Покровский В.И. Микоплазма пневмонии - инфекция. М:Медицина;1978.
5. Прозоровский С.В., Покровский В.И., Тартаковский И.С. Болезнь легионеров (легионеллез). М:Медицина; 1984.
6. Прозоровский С.В., Раковская И.В., Вульфович Ю.В. Медицинская микоплазмология. М:Медицина;1995.
7. Раковская И.В., Горина Л.Г. Лабораторная диагностика микоплазмозов человека. Клин лаб диагностика 1999;11:6 7.
8. Синопальников А.И. Рациональная антибактериальная терапия пневмоний. Рос мед вести 1996;1:5-13.
9. Тартаковский И.С., Прозоровский С.В. Оппортунистические инфекции - новая область клинической микробиологии. Рос мед вести 1997;1:46-51.
10. Эйдельштейн И.А. Фундаментальные изменения в классификации хламидий и родственных им микроорганизмов порядка Chlamydiales Клин микробиол и антимикроб химиотер 1999;1:5-11.
11. Abele Horn M., Busch U., Nitscheo, et al. Molecular approaches to diagnosis of pulmonary diseases due to M.pneumoniae. J Clin Microbiol 1998;36:548-51.
12. Dean D., Ferrero D., McCarthy M. Comparison of performance and cost-effectiveness of direct fluorescent-antibody, Ligase chain reaction and PCR assay for verification of chlamydial enzyme immunoassay results for a populations with a low to moderate prevalence of Chlamydia trachomatis infection. J Clin Microbiol 1998;36:94-9.
13. Dorigo-Zetsma L.W., Zaat S.A., Wertheim von Dillen P.M.E., et al. Comparison of PCR, culture and serological tests for diagnosis of Мicoplasma pneumoniae respiratory tract infection in children. J Clin Microbiol 1999;37:14-7.
14. Duffy M.E., Whithear K.G., et al. Indirect enzyme linked immunosorbent assay for detection of immunoglobuline G reactive with a recombinant protein-expressed for the gene encoding the 116 KD protein of M.pneumoniae . J Clin Microbiol 1999;37:1024-9.
15. Edelstein P.H., Meyer R.D. Legionella pneumophila. In:L.E. Remington ed. Respiratory infections: Diagnosis and Management. New York: Raven Press Ltd;1994.p.455-83.
16. Fournies P.E., Marrie T.L., Raoult D. Diagnosis of Q fever. J Clin Microbiol 1999;36:1823-34.
17. Grondahl B., Papper W., Hoppe A., et al. Rapid identification of nine microorganisms causing acute respiratory tract infections by single-tube multiplex reverse transcription PCR feasibility study. J Clin Microbiol 1999;37:1-7.
18. Harrison T., Uldum S., Tartakovskii I.S., et al. A multicenter evaluation of the biotest legionella urinary antigen EIA. Clin Microbiol Infect 1998;4:359-65.
19. Jantos C.A., Roggendorf R., Wupperman T.N., et al. Rapid detection of Chlamydia pneumoniae by PCR. J Clin Microbiol 1998;36:1890-94.
20. Jaulhac B., Reyrolle M., Sodahlou Y.K., et al. Comparison of sample preparation methods for detection of L.pneumophila in culture positive bronchoalveolar lavage fluids by PCR. J Clin Microbiol 1998;36:2120-2.
21. Kalin M. Atypical pneumonia agents in Scandinavia clinical importance and diagnostic aspects. In: B.P. Berdaled. Legionella infection and atypical pneumonias. Oslo, Norway; 1996.p.139-44.
22. Lindsday D., Abraham S.W.H., Fallou R.J., et al. Detection of mip gene by PCR for diagnosis of Legionaries Disease. J Clin Microbiol 1994;32:3068-9.
23. Serebrov V., Kazar J., Novkiriski N., et. al. Q-fever in Bulgaria and Slovakia. Emerg Infect Dis 1999;5:1999-2003.
24. Sinopalnikov A.I., Tartakovskii I.S. Etiologic structure of community-acquired pneumonias. EWGLI-13. Finland, Helsinki;1998.p.65.
25. Stein A., Ravult D. Detection of C burnetii by DNA amplification using PCR. J Clin Microbiol 1992;30:2462-5.
26. Talkinyton D.F., Thacker W., Keller D.W., et al. Diagnosis of M.pneumoniae infection in autopsy and open-lung biopsy tissues by Nested PCR. J Clin Microbiol 1992;36:1151-3.
27. Tartakovskii I.S., Sinopalnikov A.I., Martinova V.R., Gorina L.G. Community-acquired pneumonia: etiologic diagnosis and strategy of antibiotic therapy. In: B.P.Berdal ed. Legionella infection and atypical pneumonias. Oslo, Norway;1996.p.149-52.
28. Verkovjen R.P., Willemse D., Hiep van Casteren S.C.A.M., et al. Evaluation of PCR, culture and serology for diagnosis of C.pneumoniae respiratory infection. J Clin Microbiol 1998;36:2301-7.
29. Waris M.E., Toikka P., Saarinen T., et al. Diagnosis of M.pneumoniae in children. J Clin Microbiol 1998; 36:3155-9.
30. Zhang G.Q., Hotta A., Mizutani M., et. al. Direct identification of Coxiella burnetii plasmids in Human serum by nested PCR. J Clin Microbiol 1998;36:2210-3.
УДК 616.24-002-022-07